卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答下列问题:
(1)氟原子激发态的电子排布式有_,其中能量较高的是_。(填标号)
a.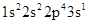
b.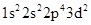
c.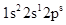
d.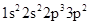
(2)①一氯乙烯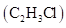 分子中,C的一个_杂化轨道与Cl的
分子中,C的一个_杂化轨道与Cl的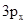 轨道形成
轨道形成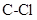 _键,并且Cl的
_键,并且Cl的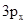 轨道与C的
轨道与C的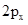 轨道形成3中心4电子的大
轨道形成3中心4电子的大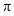 键
键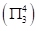 。
。
②一氯乙烷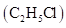 、一氯乙烯
、一氯乙烯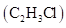 、一氯乙炔
、一氯乙炔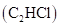 分子中,
分子中, 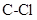 键长的顺序是_,理由:(ⅰ)C的杂化轨道中s成分越多,形成的
键长的顺序是_,理由:(ⅰ)C的杂化轨道中s成分越多,形成的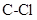 键越强:(ⅱ)_。
键越强:(ⅱ)_。
(3)卤化物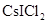 受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为_。解释X的熔点比Y高的原因_。
受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为_。解释X的熔点比Y高的原因_。
(4) 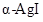 晶体中
晶体中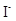 离子作体心立方堆积(如图所示),
离子作体心立方堆积(如图所示), 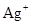 主要分布在由
主要分布在由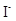 构成的四面体、八面体等空隙中。在电场作用下,
构成的四面体、八面体等空隙中。在电场作用下, 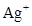 不需要克服太大的阻力即可发生迁移。因此,
不需要克服太大的阻力即可发生迁移。因此, 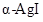 晶体在电池中可作为_。
晶体在电池中可作为_。
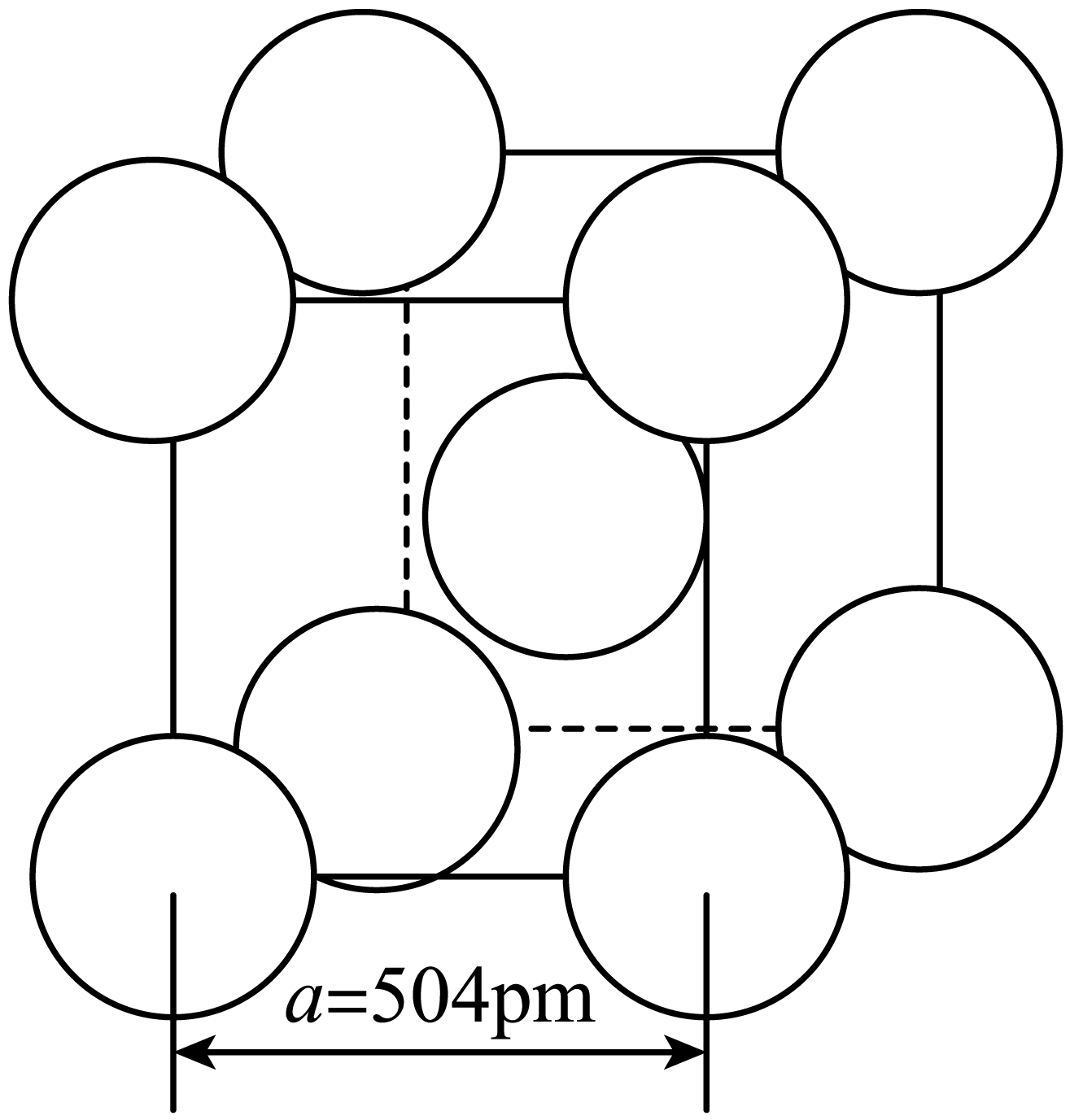
已知阿伏加德罗常数为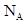 ,则
,则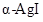 晶体的摩尔体积
晶体的摩尔体积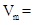 _
_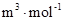 (列出算式)。
(列出算式)。
答案
(1) ①. ad ②. d
(2) ①. sp2 ②. σ ③. 一氯乙烷>一氯乙烯>一氯乙炔 ④. Cl参与形成的大π键越多,形成的C-Cl键的键长越短
(3) ①. CsCl ②. CsCl为离子晶体,ICl为分子晶体
(4) ①. 电解质 ②.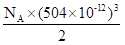
解析






